ж–Ү. и®ёжҹҜ
2 C) @8 H: x( P. y: K5 e% q; ]$ GеёёеёёжңүдәәиЎЁзӨәпјҡдҪ иҝҷж–Үз« зңӢдёҠеҺ»еҫҲвҖңй«ҳеӨ§дёҠвҖқпјҢж„ҹи§үе…¶дёӯзҡ„дҝЎжҒҜеҜ№жҲ‘д№ҹжңүзӣҠеӨ„пјҢеҸҜжҳҜжҲ‘еҚҙиҜ»дёҚжҮӮж–Үз« еҲ°еә•иҜҙдәҶд»Җд№ҲпјҢиҝҷиҜҘжҖҺд№ҲеҠһе‘ўпјҹ
9 @5 i2 E& J- l3 U. ]& e. C& z( S
еҲ«зқҖжҖҘпјҢжҺҘдёӢжқҘжҲ‘е°ҶеёҰйўҶеӨ§е®¶еӯҰд№ иҜ»жҮӮзҷҢз—Ү科жҷ®ж–Үз« зҡ„еҗ„дёӘиҰҒзӮ№пјҢеӯҰдјҡд№ӢеҗҺдҪ д№ҹеҸҜд»ҘиҪ»жқҫзңӢжҮӮзҷҢз—Үзҡ„科жҷ®ж–ҮдәҶпјҒ
& b1 ~" Z4 [+ G! s$ ~6 @$ J
иҜ•йӘҢзұ»еһӢ
; Q X% I+ ?, p# t. \- B/ @% @дёҖиҲ¬зҷҢз—Ү科жҷ®ж–Үз« еӨҡжҳҜеӣҙз»•дёҙеәҠиҜ•йӘҢеұ•ејҖзҡ„пјҢиҖҢиҝҷдәӣиҜ•йӘҢзҡ„жң¬иҙЁе°ұжҳҜйҖҡиҝҮз ”з©¶дёҚеҗҢжІ»з–—ж–№жі•зҡ„з–—ж•ҲгҖҒе®үе…ЁжҖ§зӯүй—®йўҳпјҢжүҫеҜ»еҮәжӣҙеҠ дјҳз§Җзҡ„жІ»з–—ж–№жЎҲгҖӮж—ўеҢ…жӢ¬дәҶж–°иҚҜз ”з©¶гҖҒеҸҲеҢ…жӢ¬дәҶж–°жІ»з–—ж–№жЎҲзҡ„з ”з©¶гҖӮдәҶи§ЈиҜ•йӘҢзұ»еһӢпјҢеҸҜд»ҘжңүеҠ©дәҺжҲ‘们дәҶи§ЈиҜ•йӘҢзҡ„зңҹе®һжҖ§е’ҢеҸҜйқ жҖ§гҖӮ
: \. a( d/ V5 k. a9 d/ zдёҖгҖҒжҢүз ”з©¶йҳ¶ж®өеҲҶзұ»
" x U# b2 u( k
ж №жҚ®дёҙеәҠиҜ•йӘҢзҡ„з ”з©¶йҳ¶ж®өеҸҜд»Ҙе°ҶиҜ•йӘҢеҲҶдёәв… жңҹдёҙеәҠиҜ•йӘҢпјҢв…ЎжңҹдёҙеәҠиҜ•йӘҢпјҢв…ўжңҹдёҙеәҠиҜ•йӘҢе’Ңв…ЈжңҹдёҙеәҠиҜ•йӘҢгҖӮ
0 D+ W0 A1 z5 Dв… жңҹдёҙеәҠиҜ•йӘҢдё»иҰҒжҳҜе®үе…ЁжҖ§иҜ•йӘҢпјҢжӢӣеӢҹе°‘йҮҸзҡ„еҸ—иҜ•иҖ…жқҘеҲӨе®ҡиҜ•йӘҢж–№жЎҲзҡ„е®үе…ЁжҖ§е’ҢеҸҜе®ҢжҲҗжҖ§пјҢиҜ„д»·иҜ•йӘҢж–№жЎҲеңЁжӮЈиҖ…дёӯзҡ„иҖҗеҸ—зЁӢеәҰе’Ңз—…зҗҶеӯҰеҸҚеә”пјҢдёәд№ӢеҗҺиҜ•йӘҢж–№жЎҲзҡ„еҲ¶е®ҡжҸҗдҫӣдҫқжҚ®гҖӮжӯӨйҳ¶ж®өеӨ§зәҰйңҖиҰҒеҮ еҚҒдәәеҸӮдёҺгҖӮ
* w1 f, E8 `& a' S* A, P# `
в…ЎжңҹдёҙеәҠиҜ•йӘҢеҜ№з ”究方жЎҲзҡ„з–—ж•Ҳе’Ңе®үе…ЁжҖ§иҝӣиЎҢеҲқжӯҘзҡ„иҜ„дј°пјҢејҖе§Ӣдә§еҮәеҲқжӯҘзҡ„иҜ•йӘҢз»“жһңпјҢеҗҢж—¶еҜ№ж–°ж–№жЎҲжІ»з–—иҝҮзЁӢдёӯз–ҫз—…зҡ„еҸ‘еұ•иҝӣиЎҢз ”з©¶гҖӮ继з»ӯдёәеҗҺз»ӯе®һйӘҢж–№жЎҲзҡ„еҲ¶е®ҡжҸҗдҫӣеҸӮиҖғе’ҢдҫқжҚ®гҖӮиҜҘйҳ¶ж®өиҜ•йӘҢйҖҡеёёйңҖиҰҒдёҠзҷҫдәәгҖӮ
9 d& {/ }( V& \' D. s' iв…ўжңҹдёҙеәҠиҜ•йӘҢе°ҶжңҖз»ҲзЎ®е®ҡжІ»з–—ж–№жЎҲзҡ„жІ»з–—жҲҗжһңгҖӮиҝӣдёҖжӯҘйӘҢиҜҒжІ»з–—ж–№жЎҲзҡ„з–—ж•ҲдёҺе®үе…ЁжҖ§гҖӮдёәж–°зҡ„жІ»з–—ж–№жЎҲзҡ„жіЁеҶҢе®Ўжү№жҸҗдҫӣдҫқжҚ®гҖӮйңҖиҰҒеҮ зҷҫиҮіеҮ еҚғеҗҚеҸ—иҜ•иҖ…иҝӣиЎҢз»јеҗҲзҡ„иҖғйҮҸгҖӮ
' E: I$ }# V4 Q: U5 O$ mв…ЈжңҹдёҙеәҠиҜ•йӘҢдёәжІ»з–—ж–№жЎҲиҺ·жү№еҗҺзҡ„дёҙеәҠз ”з©¶гҖӮиҜ„дј°жІ»з–—ж–№жЎҲеңЁе№ҝжіӣдҪҝз”ЁжқЎд»¶дёӢзҡ„жІ»з–—ж•Ҳжһңе’Ңе®үе…ЁжҖ§пјҢиҜ„д»·еңЁжҷ®йҖҡе’Ңзү№ж®ҠдәәзҫӨдёӯдҪҝз”Ёзҡ„иҺ·зӣҠдёҺйЈҺйҷ©е…ізі»пјҢеҲӨж–ӯжҳҜеҗҰиҰҒжӣҙж”№дҪҝз”ЁеүӮйҮҸзӯүгҖӮ
8 T& r3 `3 t( S" ~
дёҙеәҠиҜ•йӘҢеҲҶжңҹеӣҫ
h9 @; o$ t; f1 Y2 @ ^4 W" gдәҢгҖҒжҢүиҜ•йӘҢ规模еҲҶзұ»
' l! g. e+ c1 U* wеҰӮжһңиҜҘдёҙеәҠиҜ•йӘҢж ·жң¬дәәж•°еңЁ1000дәәд»ҘдёҠеҲҷз§°дёәеӨ§ж ·жң¬дёҙеәҠиҜ•йӘҢпјҢеҸҚд№ӢеҲҷз§°дёәе°Ҹж ·жң¬дёҙеәҠе®һйӘҢгҖӮеӨ§ж ·жң¬иҜ•йӘҢеҰӮжһңж¶өзӣ–еӨҡ家еҢ»з–—жңәжһ„йҒҚеёғеҗ„ең°з”ҡиҮійҒҚеёғеҗ„еӣҪпјҢеҲҷз§°дёәеӨ§ж ·жң¬еӨҡдёӯеҝғдёҙеәҠиҜ•йӘҢгҖӮжӯӨзұ»иҜ•йӘҢиҖғеҜҹдәәж•°еӨҡпјҢеҸ—иҜ•дәәе‘ҳеӨҡж ·пјҢиҖ—ж—¶иҫғй•ҝеӣ жӯӨжүҖеҫ—еҲ°зҡ„з»“и®әйҖҡеёёиҫғдёәеҮҶзЎ®пјҢжҜ”иҫғжңүиҜҙжңҚеҠӣгҖӮ
( l* t' t; x* S: NдёүгҖҒжҢүиҜ•йӘҢеҜ№з…§и®ҫзҪ®еҲҶзұ»
. c# H) s5 |1 @& g% G# q% `* J
еҸӘиҝӣиЎҢе®һйӘҢж–№жЎҲзҡ„и®әиҜҒпјҢжІЎжңүи®ҫзҪ®еҜ№з…§з»„зҡ„дёҙеәҠиҜ•йӘҢиў«з§°дёәеҚ•иҮӮиҜ•йӘҢпјӣ
) y' U& o4 P* u3 E' k4 b
иҖҢеҸҢиҮӮиҜ•йӘҢе°ұжҳҜжҢҮи®ҫзҪ®дәҶе№іиЎҢзҡ„е…¶д»–ж–№жЎҲжҲ–еҜ№з…§з»„зҡ„иҜ•йӘҢпјӣ
l& X" o' W( m" e7 Z; y
дёүиҮӮиҜ•йӘҢеҲҷжҳҜйҷӨеҜ№з…§з»„еӨ–иҝҳи®ҫзҪ®дәҶе®үж…°еүӮз»„гҖӮи®ҫзҪ®еҜ№з…§з»„зҡ„иҜ•йӘҢдёәзЎ®дҝқиҜ•йӘҢзҡ„еҮҶзЎ®пјҢеҲҶз»„и®ҫзҪ®дёҖиҲ¬дёәйҡҸжңәеҲҶй…ҚгҖӮ
^2 n3 w8 Y3 r5 Q7 \/ O$ e
еӣӣгҖҒжҢүеҸ—иҜ•иҖ…зҹҘжғ…жғ…еҶөеҲҶзұ»
, B, q0 ? D$ [# w; Yж №жҚ®еҸ—иҜ•иҖ…еҜ№дәҺж•ҙдёӘиҜ•йӘҢзҡ„дәҶи§Јжғ…еҶөеҸҜе°ҶиҜ•йӘҢеҲҶдёәеҚ•зӣІгҖҒеҸҢзӣІе’ҢдёүзӣІгҖӮ
; d" z2 e/ j3 v9 @. h+ |+ i5 X
еҚ•зӣІиҜ•йӘҢжҳҜжҢҮеҸ—иҜ•иҖ…зҹҘйҒ“иҮӘе·ұзҡ„еҲҶз»„жғ…еҶөпјҢдҪҶдёҚзҹҘйҒ“дёӘеҲ«дјҡеј•иө·дёӘдәәеҒҸеҘҪзҡ„дҝЎжҒҜпјҢиҖҢе®һйӘҢдәәе‘ҳе®Ңе…ЁжҺҢжҸЎиҜ•йӘҢзҡ„е…ЁйғЁдҝЎжҒҜпјӣ
: P1 E' ?, Y+ d, \
еҸҢзӣІиҜ•йӘҢжҳҜжҢҮеҸ—иҜ•иҖ…е’Ңе®һйӘҢдәәе‘ҳйғҪдёҚзҹҘйҒ“еҸ—иҜ•иҖ…зҡ„еҲҶз»„жғ…еҶөпјҢеҸӘжңүж•°жҚ®и®°еҪ•е®ҢжҜ•еҗҺе®һйӘҢдәәе‘ҳжүҚзҹҘйҒ“дәәе‘ҳеҲҶз»„гҖӮеҸҢзӣІиҜ•йӘҢжҜ”иө·еҚ•зӣІиҜ•йӘҢжӣҙеҠ дёҘж јпјҢеҸҜд»Ҙж¶ҲйҷӨеҸ—иҜ•дәәе‘ҳе’ҢиҜ•йӘҢдәәе‘ҳеӣ дё»и§Ӯж„ҸиҜҶеҸҠдёӘдәәеҒҸеҘҪйҖ жҲҗзҡ„з»“жһңеҒҸе·®пјҢжҳҜз»қеӨ§еӨҡж•°иҜ•йӘҢдјҡйҮҮеҸ–зҡ„ж–№жі•пјӣ
* ^& U. l5 O) H' Y4 s4 r% Y
дёүзӣІиҜ•йӘҢжҳҜеҸ—иҜ•дәәе‘ҳгҖҒиҜ•йӘҢдәәе‘ҳе’ҢеҲҶжһҗдәәе‘ҳйғҪдёҚзҹҘйҒ“е…·дҪ“зҡ„дәәе‘ҳеҲҶз»„гҖӮиҝҷз§Қжғ…еҶөиҷҪ然иғҪеңЁжңҖеӨ§зЁӢеәҰдёҠйҒҝе…ҚдёӘдәәеҒҸеҘҪйҖ жҲҗзҡ„иҜҜе·®пјҢдҪҶеҜ№иҜ•йӘҢзҡ„е®үе…ЁжҖ§иҰҒжұӮеҫҲй«ҳпјҢжү§иЎҢиө·жқҘд№ҹжӣҙдёәеӨҚжқӮгҖӮ
. G$ v( {! o. E) j) q5 \, \4 s
дә”гҖҒж №жҚ®иҜ•йӘҢйҮҮз”Ёж–№жі•еҲҶзұ»
+ ?) h3 y- C' K( S0 P& ~1 fз ”з©¶дәәе‘ҳж №жҚ®еҒҮи®ҫи®ҫи®Ўе®һйӘҢ并йӘҢиҜҒеҒҮи®ҫз§°дёәеүҚзһ»жҖ§иҜ•йӘҢпјӣз ”з©¶дәәе‘ҳж №жҚ®е·Іжңүзҡ„ж•°жҚ®и®ҫи®Ўе®һйӘҢжүҫеҮәж•°жҚ®дә§з”ҹзҡ„еҺҹеӣ иў«з§°дёәеӣһйЎҫжҖ§иҜ•йӘҢгҖӮз®ҖеҚ•зӮ№зҗҶи§ЈеүҚзһ»жҖ§иҜ•йӘҢе°ұжҳҜз”ұеӣ жәҜжһңпјҢеӣһйЎҫжҖ§иҜ•йӘҢжҳҜз”ұжһңиҝҪеӣ гҖӮ
- x- g7 w) L1 G4 X- X/ M
ж–°иҚҜгҖҒж–°еһӢжІ»з–—ж–№жЎҲз–—ж•ҲиҜ„е®ҡзҡ„иҜ•йӘҢдёҖиҲ¬еұһдәҺеүҚзһ»жҖ§иҜ•йӘҢпјҢз ”з©¶жӮЈиҖ…еҸ‘з—…еҺҹеӣ е’ҢеҸ‘з—…жңәзҗҶзҡ„иҜ•йӘҢйҖҡеёёдёәеӣһйЎҫжҖ§иҜ•йӘҢгҖӮ
5 v G9 t1 a4 l3 E ?з–—ж•ҲиҜ„д»·жҢҮж Ү
' o# D# A4 _6 y: X v# xзңӢжҮӮ科жҷ®ж–Үз« жңҖеӨ§зҡ„йҡҫзӮ№е°ұжҳҜеҗ„з§Қе…ідәҺз–—ж•ҲиҜ„дј°зҡ„иӢұж–Үзј©еҶҷпјҢиҜёеҰӮOSгҖҒPFSгҖҒORRзӯүпјҢе®ғ们еҲ°еә•жңүд»Җд№Ҳеҗ«д№үпјҹе®ғ们еңЁжІ»з–—ж•Ҳжһңзҡ„иҜ„д»·дёӯеҸҲиғҪиҜҙжҳҺд»Җд№Ҳе‘ўпјҹжҲ‘еңЁиҝҷйҮҢдёәеӨ§е®¶жҖ»з»“еҮәжқҘиӮҝзҳӨжІ»з–—дёӯеёёи§Ғзҡ„з–—ж•ҲиҜ„д»·жҢҮж ҮпјҢеӨ§е®¶жӢҝе°Ҹжң¬жң¬и®°еҘҪдәҶпјҒ
9 b% F& Z2 J \3 q1 cдёҖгҖҒз”ҹеӯҳиҺ·зӣҠз–—ж•ҲиҜ„д»·жҢҮж Ү
1. OSпјҲOverall SurvivalпјүпјҡжҖ»з”ҹеӯҳжңҹ
жҢҮзҡ„жҳҜдёҙеәҠиҜ•йӘҢдёӯжӮЈиҖ…д»ҺйҡҸжңәеҢ–ејҖе§ӢиҮіеӣ д»»дҪ•еҺҹеӣ еј•иө·зҡ„жӯ»дәЎж—¶й—ҙгҖӮзӣҙзҷҪзӮ№иҜҙе°ұжҳҜжҺҘеҸ—иҜ•йӘҢзҡ„жӮЈиҖ…д»ҺиҜ•йӘҢејҖе§ӢзӣҙиҮіжӯ»дәЎзҡ„жҖ»ж—¶й—ҙпјҢеҰӮжһңжӮЈиҖ…еңЁз ”究结жқҹж—¶д»Қ然еӯҳжҙ»пјҢеҲҷдёәе®һйӘҢејҖе§ӢеҲ°жңҖеҗҺдёҖж¬ЎйҡҸи®ҝзҡ„ж—¶й—ҙгҖӮ
. z0 P5 k) ]1 O$ v( m
OSиў«и®ӨдёәжҳҜиӮҝзҳӨдёҙеәҠиҜ•йӘҢдёӯжңҖдҪізҡ„з–—ж•Ҳз»ҲзӮ№пјҢеҪ“жӮЈиҖ…зҡ„з”ҹеӯҳжңҹиғҪе……еҲҶиҜ„дј°ж—¶пјҢе®ғжҳҜйҰ–йҖүз»ҲзӮ№гҖӮе®ғжңҖеӨ§зҡ„дјҳзӮ№жҳҜи®°еҪ•ж–№дҫҝпјҢжңҖеӨ§зҡ„зјәзӮ№жҳҜеңЁеӨ§еһӢдёҙеәҠиҜ•йӘҢдёӯйҡҸи®ҝж—¶й—ҙиҫғй•ҝгҖӮжүҖд»ҘдёҙеәҠдёҠеёёдҪҝз”Ё5е№ҙз”ҹеӯҳзҺҮпјҢеҚіжҹҗдёҖз§ҚиӮҝзҳӨз»ҸиҝҮз»јеҗҲжІ»з–—еҗҺпјҢз”ҹеӯҳжңҹи¶…иҝҮ5е№ҙзҡ„жӮЈиҖ…жҜ”дҫӢгҖӮ
7 W. [9 i$ X% j. c( Z
2. PFSпјҲProgress Free Survivalпјүпјҡж— иҝӣеұ•з”ҹеӯҳжңҹ
жҢҮд»ҺйҡҸжңәеҢ–дёҙеәҠиҜ•йӘҢејҖе§ӢеҲ°иӮҝзҳӨеҸ‘з”ҹпјҲд»»дҪ•ж–№йқўпјүиҝӣеұ•жҲ–еӣ д»»дҪ•еҺҹеӣ еҜјиҮҙжӯ»дәЎзҡ„ж—¶й—ҙгҖӮд№ҹе°ұжҳҜеҸ—иҜ•иҖ…еңЁиҜ•йӘҢж–№жЎҲжІ»з–—зҡ„жқЎд»¶дёӢпјҢиӮҝзҳӨеҶҚеәҰз”ҹй•ҝжүҖйңҖзҡ„ж—¶й—ҙгҖӮ
. |3 s5 h6 }* l0 k
PFSд№ҹжҳҜжҷҡжңҹиӮҝзҳӨиҜ•йӘҢз–—ж•ҲиҜ„д»·зҡ„йҮҚиҰҒжҢҮж ҮпјҢйҮҚиҰҒзЁӢеәҰд»…ж¬ЎдәҺOSгҖӮ
' p2 }5 _3 ?3 \3. DFSпјҲDisease Free Survivalпјүпјҡж— з—…з”ҹеӯҳжңҹ
жҢҮд»ҺйҡҸжңәеҢ–ејҖе§ӢиҮіз¬¬дёҖж¬ЎиӮҝзҳӨеӨҚеҸ‘/иҪ¬з§»жҲ–з”ұдәҺд»»дҪ•еҺҹеӣ еҜјиҮҙеҸ—иҜ•иҖ…жӯ»дәЎзҡ„ж—¶й—ҙгҖӮ
& ]% C9 H1 x: N5 L( f: w. ^
иҜҘжҢҮж Үдё»иҰҒз”ЁдәҺж №жІ»жүӢжңҜеҗҺзҡ„з–—ж•ҲиҜ„еҲӨпјҢж–°иҚҜжҲ–ж–°еһӢжІ»з–—ж–№ејҸиҜ•йӘҢдёҖиҲ¬дёҚдҪҝз”ЁиҜҘжҢҮж ҮгҖӮ
! e/ O6 L1 Q. Y( }: ~
еҰӮжһңеңЁOSгҖҒPFSе’ҢDFSеүҚйқўеҠ дёҠдёҖдёӘе°ҸеҶҷзҡ„mпјҢиЎЁзӨәдёӯдҪҚж—¶й—ҙпјҢеҰӮmOSиЎЁзӨәдёӯдҪҚз”ҹеӯҳжңҹпјҢеҚіжҒ°еҘҪжңү50пј…зҡ„дёӘдҪ“е°ҡеӯҳжҙ»зҡ„ж—¶й—ҙгҖӮеҸҜд»ҘзңӢеҒҡжҳҜOSзҡ„е№іеқҮеҖјгҖӮ
: F0 K. R! x0 A5 t5 e5 t' t$ F
4. TTPпјҲTime To Progressпјүпјҡз–ҫз—…иҝӣеұ•ж—¶й—ҙ
жҢҮд»ҺйҡҸжңәеҲҶз»„ејҖе§ӢеҲ°з¬¬дёҖж¬ЎиӮҝзҳӨе®ўи§Ӯиҝӣеұ•зҡ„ж—¶й—ҙгҖӮ
: k) _' n2 `: R$ i- f
TTPдёҺPFSзӣёдјјпјҢе”ҜдёҖдёҚеҗҢеңЁдәҺPFSеҢ…жӢ¬жӯ»дәЎгҖӮеӣ жӯӨPFSдҪҝз”Ёжӣҙе№ҝжіӣпјҢжӣҙиғҪйў„жөӢе’ҢеҸҚеә”дёҙеәҠ收зӣҠпјҢдёҺOSдёҖиҮҙжҖ§жӣҙеҘҪгҖӮеңЁеҜјиҮҙжӯ»дәЎзҡ„йқһиӮҝзҳӨеҺҹеӣ еӨҡдәҺиӮҝзҳӨеҺҹеӣ зҡ„жғ…еҶөдёӢпјҢTTPжҳҜдёҖдёӘеҗҲйҖӮзҡ„жҢҮж ҮгҖӮ
" W1 n/ p5 K' x! W7 ^( v( |
дәҢгҖҒиӮҝзҳӨеҸҚеә”з–—ж•ҲиҜ„д»·жҢҮж Ү
1 y/ G3 o) _ q5 D S0 }) T
1. ORRпјҲObjective response rateпјүпјҡе®ўи§Ӯзј“и§ЈзҺҮ
жҢҮиӮҝзҳӨзј©е°ҸиҫҫеҲ°дёҖе®ҡйҮҸ并且дҝқжҢҒдёҖе®ҡж—¶й—ҙзҡ„з—…дәәзҡ„жҜ”дҫӢпјҢеҢ…еҗ«е®Ңе…Ёзј“и§ЈпјҲCRпјүе’ҢйғЁеҲҶзј“и§ЈпјҲPRпјүзҡ„з—…дҫӢгҖӮ
u" `, ]7 a, y0 H4 Z7 C; I/ X$ S
е®ўи§Ӯзј“и§ЈзҺҮдёҖиҲ¬жҳҜIIжңҹиҜ•йӘҢзҡ„дё»иҰҒз–—ж•ҲиҜ„д»·жҢҮж ҮпјҢеҸҜд»ҘеҸҚеә”иҚҜзү©зҡ„з”ҹзү©жҙ»жҖ§гҖӮ
- T* @& S& L, U4 n2 n" s7 q2. DCRпјҲDisease Control Rateпјүпјҡз–ҫз—…жҺ§еҲ¶зҺҮ
жҢҮиӮҝзҳӨзј©е°ҸжҲ–зЁіе®ҡдё”дҝқжҢҒдёҖе®ҡж—¶й—ҙзҡ„з—…дәәзҡ„жҜ”дҫӢпјҢеҢ…еҗ«е®Ңе…Ёзј“и§ЈпјҲCRпјүгҖҒйғЁеҲҶзј“и§ЈпјҲPRпјүе’Ңз–ҫз—…зЁіе®ҡпјҲSDпјүзҡ„з—…дҫӢгҖӮ
q( ?4 f0 W+ w/ Y& L; m$ Hдё»иҰҒжҳҜй’ҲеҜ№е®һдҪ“иӮҝзҳӨзҡ„жҢҮж ҮгҖӮ
! c2 x$ V' m0 Z; y! Z( t' W0 J3. DORпјҲDuration of Responseпјүпјҡзј“и§ЈжҢҒз»ӯж—¶й—ҙ
жҢҮиӮҝзҳӨ第дёҖж¬ЎиҜ„дј°дёәе®Ңе…Ёзј“и§ЈпјҲCRпјүжҲ–йғЁеҲҶзј“и§ЈпјҲPRпјүејҖе§ӢеҲ°з¬¬дёҖж¬ЎиҜ„дј°дёәзЁӢеәҸжҖ§жӯ»дәЎпјҲPDпјүжҲ–д»»дҪ•еҺҹеӣ жӯ»дәЎзҡ„ж—¶й—ҙгҖӮ
" p# c/ I2 N! c' Z8 S$ U' L
жҳҜиҜ„д»·з–—ж•Ҳзҡ„дёҖдёӘеҸҜеҸӮиҖғжҢҮж ҮпјҢдҪҝз”ЁиҫғдёәзҪ•и§Ғ
! ]8 V5 A1 Y. }# v* L/ F( N3 R
4. TTFпјҲTime To FailureпјүпјҡжІ»з–—еӨұиҙҘж—¶й—ҙ
жҢҮд»ҺйҡҸжңәеҢ–ејҖе§ӢиҮіжІ»з–—дёӯжӯў/з»Ҳжӯўзҡ„ж—¶й—ҙпјҢеҢ…жӢ¬д»»дҪ•дёӯжӯў/з»ҲжӯўеҺҹеӣ пјҢеҰӮз–ҫз—…иҝӣеұ•гҖҒжӯ»дәЎгҖҒз”ұдәҺдёҚиүҜдәӢ件йҖҖеҮәгҖҒеҸ—иҜ•иҖ…жӢ’з»қ继з»ӯиҝӣиЎҢз ”з©¶жҲ–иҖ…дҪҝз”ЁдәҶж–°жІ»з–—зҡ„ж—¶й—ҙгҖӮ
% [3 q$ T- c, a' I1 j0 e/ M7 @6 O
иҜҘжҢҮж Үз»јеҗҲдәҶжңүж•ҲжҖ§е’ҢжҜ’жҖ§зҡ„иҜ„д»·пјҢжҳҜдёҖдёӘз»јеҗҲжҖ§зҡ„иҜ„дј°жҢҮж ҮпјҢеҸҜд»ҘиҜ„ж–ӯе®һйӘҢзҡ„е®үе…ЁжҖ§гҖӮ
& X$ ~6 d7 F- [/ C. `3 t6 M% B: _7 _( wдёүгҖҒз»ҹи®ЎеӯҰеҸӮж•°
1. HRпјҲhazard ratioпјүпјҡйЈҺйҷ©жҜ”
пј»HR=жҡҙйңІз»„зҡ„йЈҺйҷ©еҮҪж•°h1(t)/йқһжҡҙйңІз»„зҡ„йЈҺйҷ©еҮҪж•°h2(t)пјҢtжҢҮеңЁзӣёеҗҢзҡ„ж—¶й—ҙзӮ№дёҠпјҪ
5 `5 Y9 k; o+ O9 Y4 K' F1 c2. CLпјҲconfidence intervalпјүпјҡзҪ®дҝЎеҢәй—ҙ
еҚіжҢүдёҖе®ҡзҡ„жҰӮзҺҮдј°и®ЎжҖ»дҪ“еҸӮж•°жүҖеңЁзҡ„иҢғеӣҙпјҢиҜҘиҢғеӣҙз§°дёәзҪ®дҝЎгҖӮеёёеҸ–95%е’Ң99%гҖӮеҰӮ95%зҡ„зҪ®дҝЎеҢәй—ҙпјҢе°ұжҳҜд»Һиў«дј°и®Ўзҡ„жҖ»дҪ“дёӯйҡҸжңәжҠҪеҸ–еҗ«йҮҸдёәn зҡ„ж ·жң¬пјҢз”ұжҜҸдёҖдёӘж ·жң¬и®Ўз®—дёҖдёӘеҸҜдҝЎеҢәй—ҙпјҢзҗҶи®әдёҠе…¶дёӯжңү95%зҡ„еҸҜиғҪжҖ§пјҲжҰӮзҺҮпјүе°ҶеҢ…еҗ«иў«дј°и®Ўзҡ„еҸӮж•°гҖӮ
* W. I t6 V2 r3. P
PеҖјжҢҮзҡ„жҳҜжҜ”иҫғзҡ„дёӨиҖ…зҡ„е·®еҲ«пјҢз”ЁжқҘеҲӨе®ҡеҒҮи®ҫз»“жһңгҖӮPеҖји¶Ҡе°ҸпјҢи¶ҠжңүзҗҶз”ұи®ӨдёәеҜ№жҜ”дәӢзү©й—ҙеӯҳеңЁе·®ејӮгҖӮдҫӢеҰӮпјҢP<0.05,е°ұжҳҜиҜҙз»“жһңжҳҫзӨәзҡ„е·®еҲ«жҳҜз”ұжңәйҒҮжүҖиҮҙзҡ„еҸҜиғҪжҖ§дёҚи¶і5%пјҢжҲ–иҖ…иҜҙпјҢеҲ«дәәеңЁеҗҢж ·зҡ„жқЎд»¶дёӢйҮҚеӨҚеҗҢж ·зҡ„з ”з©¶пјҢеҫ—еҮәзӣёеҸҚз»“и®әзҡ„еҸҜиғҪжҖ§дёҚи¶і5%гҖӮ
. \8 E$ E! U5 [: H4 E: [HRе’ҢCLеҜ№дәҺжҲ‘们зҗҶи§ЈиҜ•йӘҢз»“жһңжІЎжңүеӨӘеӨ§зҡ„её®еҠ©пјҢжҲ‘们主иҰҒзңӢPеҖјгҖӮиӢҘPеҖјпјһ0.05пјҢеҲҷиЎЁзӨәдёӨз»„й—ҙе·®еҲ«дёҚжҳҫи‘—пјҢжІЎжңүз»ҹи®ЎеӯҰж„Ҹд№үпјӣ0.01пјңPеҖјпјң0.05пјҢиЎЁзӨәе·®еҲ«жҳҫи‘—пјӣиӢҘPпјң0.01еҲҷиЎЁзӨәе·®еҲ«йқһеёёжҳҫи‘—гҖӮ
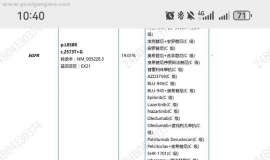
8 X5 t: j: Y6 C/ @) @* m! Sе®һжҲҳи§ЈиҜ»пјҡ
еңЁд№ӢеүҚзҡ„ж–Үз« дёӯеҮәзҺ°дәҶиҝҷж ·дёҖз»„ж•°жҚ®пјҢжҲ‘们еҸҜд»ҘзңӢеҲ°еңЁBRCAзӘҒеҸҳжӮЈиҖ…дёӯPCbз»„дёҺCEF-Tз»„зҡ„еҜ№жҜ”жғ…еҶөпјҢPеҖјдёә0.14пјҢеӨ§дәҺдәҶ0.05пјҢиҜҙжҳҺиҝҷдёӨз»„й—ҙ并没жңүд»Җд№Ҳе·®еҲ«пјҢд№ҹе°ұжҳҜиҜҙеңЁBRCAзӘҒеҸҳжӮЈиҖ…дёӯдёӨз§ҚжІ»з–—ж–№жЎҲеҜ№дәҺжӮЈиҖ…еңЁжӯ»дәЎйЈҺйҷ©дёҠзҡ„收зӣҠеҹәжң¬зӣёеҗҢгҖӮ
) O! [, G" t7 S# h. r7 I+ y# U
еӣӣгҖҒеӣҫзүҮ
1 [4 v: x0 t1 s
1. жӣІзәҝеӣҫ
: E9 S8 ]' b. U h/ ? T
7 _, H/ Q( `+ |# I- [
жӣІзәҝеӣҫйҖҡеёёйқһеёёз®ҖеҚ•жҳ“жҮӮпјҢдёҖиҲ¬еӣҫдёӯйғҪдјҡж ҮзӨәеҮәжҳҜе“Әз§ҚжӣІзәҝеӣҫпјҢдёҠеӣҫжҲ‘们еҸҜд»ҘзңӢеҲ°жҳҜPFSжӣІзәҝеӣҫгҖӮжЁӘеқҗж ҮиЎЁзӨәж—¶й—ҙеҚ•дҪҚпјҡжңҲпјҢзәөеқҗж ҮиЎЁзӨәиӮҝзҳӨжІЎжңүеҸ‘з”ҹиҝӣеұ•зҡ„дәәж•°зҷҫеҲҶжҜ”пјҢд»Һйӣ¶зӮ№ејҖе§ӢйғҪжҳҜ100%пјҢд»Һ第八дёӘжңҲејҖе§ӢпјҢзәўиүІзәҝпјҲиҒ”еҗҲз»„пјүеҸ‘з”ҹиҝӣеұ•зҡ„дәәж•°ејҖе§ӢеӨҡдәҺи“қиүІзәҝпјҲеҚ•иҚҜз»„пјүгҖӮиҜҙжҳҺ8дёӘжңҲд№ӢеҗҺеҚ•иҚҜз»„PFS收зӣҠжӣҙеҘҪгҖӮ
z6 P n; s) H2. зҖ‘еёғеӣҫ
0 U- C: }# m) u0 ^/ @
зҖ‘еёғеӣҫеҸҜд»Ҙйқһеёёжё…жҷ°зҡ„зңӢеҮәиӮҝзҳӨеӨ§е°Ҹзҡ„еҸҳеҢ–гҖӮеҰӮеӣҫжЁӘеқҗж ҮиЎЁзӨәдәәж•°пјҢзәөеқҗж ҮиЎЁзӨәиӮҝзҳӨеҸҳеҢ–пјҢеҫҖдёҠиЎЁзӨәеўһеӨ§пјҢеҫҖдёӢиЎЁзӨәеҮҸе°ҸпјҢжӯӨеӣҫжҳҫзӨәзҡ„жҳҜиӮҝзҳӨйҡҸдәәзҫӨзҡ„еҸҳеҢ–гҖӮеҰӮжһңжЁӘеқҗж ҮиЎЁзӨәж—¶й—ҙпјҢеҲҷеҸҜд»ҘзңӢеҮәиӮҝзҳӨйҡҸж—¶й—ҙзҡ„еҸҳеҢ–гҖӮ
$ r& C& |, R( @5 p, r! K
е®үе…ЁжҖ§иҜ„д»·
& M' i( g+ V; o, {+ b* I T
ж №жҚ®дёҚиүҜеҸҚеә”зЁӢеәҰеҸҜе°ҶиҚҜе“ҒеҲҶдёәеӣӣдёӘзӯүзә§пјҡв… зә§дёәиҪ»еәҰпјҢз—…дәәеҸҜд»ҘеҝҚеҸ—пјҢдёҚйңҖиҰҒеҒңиҚҜжҲ–иҖ…еҮҸйҮҸпјҢз»ҸиҝҮдёҖиҲ¬зҡ„еҜ№з—ҮеӨ„зҗҶжҲ–иҖ…дёҚйңҖиҰҒеӨ„зҗҶеҚіеҸҜд»Ҙиҫғеҝ«жҒўеӨҚпјҢдё”еҜ№з—…дәәзҡ„еә·еӨҚжІЎжңүзӣҙжҺҘеҪұе“ҚиҖ…пјӣв…Ўзә§дёәдёӯеәҰеҸҚеә”пјҢз—…дәәйҡҫд»ҘеҝҚеҸ—пјҢиў«иҝ«еҒңиҚҜжҲ–иҖ…еҮҸиҚҜпјҢз»ҸиҝҮдёҖиҲ¬зҡ„еҜ№з—ҮеӨ„зҗҶеҗҺеҸҜеҘҪиҪ¬пјҢдё”еҜ№з—…дәәзҡ„еә·еӨҚжІЎжңүзӣҙжҺҘеҪұе“ҚиҖ…пјӣв…ўзә§дёәйҮҚеәҰеҸҚеә”пјҢз—…дәәеҸҚеә”з—ҮзҠ¶жҳҺжҳҫпјҢжңүеҗ„еҷЁе®ҳз—…зҗҶз”ҹзҗҶж”№еҸҳжҲ–иҖ…жЈҖйӘҢејӮеёёпјҢиў«иҝ«ж’ӨиҚҜпјҢ并且йңҖиҰҒеҒҡзү№ж®ҠеӨ„зҗҶпјҢеҜ№з—…дәәзҡ„еә·еӨҚе·Із»Ҹдә§з”ҹзӣҙжҺҘеҪұе“ҚпјҢжҲ–иҖ…дёҚиүҜеҸҚеә”жҢҒз»ӯ7еӨ©д»ҘдёҠиҖ…пјӣв…Јзә§дёәдёҘйҮҚеҸҚеә”пјҢзӣҙжҺҘиҮҙжӯ»жҲ–жҳҜдҝғиҝӣжӯ»дәЎпјҢйңҖиҰҒз«ӢеҚіж’ӨиҚҜ并且еҒҡеҮәзҙ§жҖҘеӨ„зҗҶгҖӮ
/ R+ K" L" N6 K% Z
' }/ y- h9 D9 c$ ?, a/ ^" ^7 a( I: e
еҰӮжһңеӨ§е®¶еңЁйҳ…иҜ»зҷҢз—Ү科жҷ®ж–Үз« ж—¶иҝҳжңүд»Җд№Ҳеӣ°йҡҫжҲ–дёҚжҳҺзҷҪзҡ„ең°ж–№пјҢж¬ўиҝҺеӨ§е®¶еңЁиҜ„и®әдёӯжҢҮеҮәпјҒ